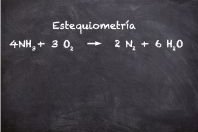Masa Molar
Qué es la masa molar:
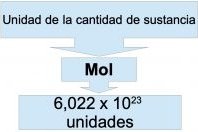
La masa molar (M) es la cantidad de masa que una sustancia contiene en un mol. Un mol se define como 6.022 x10 23 partículas.
En química, la masa molar es importante para determinar la cantidad de masa de una sustancia. Es por ello que la masa molar es expresada generalmente por gramos por mol (g/mol).
En la tabla periódica, se puede encontrar la masa molar de los elementos, también llamada masa atómica o peso atómico, en la parte inferior del elemento. Por ejemplo, el hidrógeno tiene una masa molar de 1.008 gr/mol y el nitrógeno de 14.01 gr/mol.
Para calcular la masa molar de un compuesto, también llamado peso molecular, se debe sumar la masa molar de los elementos del compuesto multiplicado por las veces que aparecen, por ejemplo:
Cuando se conoce la masa molar de un compuesto, se sabe a su vez la cantidad de mol por gramo, recordando que cada mol es 6.022 x 1023 partículas.
Por lo tanto, conociendo la masa molar se podrá calcular la cantidad de moles usando la fórmula:
mol= masa / masa molar.
Por ejemplo, en 100 gramos de amoniaco (NH3) para encontrar la cantidad de moles debemos dividir 100 / 17.03 g/mol que da un resultado aproximado de 5.8 moles en 100 gramos de amoniaco.
Vea también:
Cómo citar: (09/02/2023). "Masa Molar". En: Significados.com. Disponible en: https://www.significados.com/masa-molar/ Consultado: