Electrón
El electrón es una partícula subatómica y elemental que orbita alrededor del núcleo atómico. Esta partícula está ubicada en orbitales y se posiciona en diferentes niveles energéticos según la energía que tenga.
Los electrones, de símbolo e-, presentan una carga negativa aproximada de −1,602176 x 10-19 culombios, y una masa alrededor de 9,1 × 10−31 kg. Al ser partículas elementales, son indivisibles, por lo que no se descomponen en otras ni poseen subestructuras.
El electrón es una partícula que orbita alrededor del núcleo del átomo en regiones determinadas y niveles energéticos distintos.
Los electrones son fundamentales en la formación de los enlaces químicos, y por ende, de las reacciones químicas. Las moléculas se forman gracias a estas partículas, de acuerdo con la electronegatividad de los átomos y la presencia de la polaridad.
Además, los electrones no están fijos, sino que presentan un comportamiento ondulatorio. También se pueden hallar libres, fuera de los átomos, y desplazarse en el espacio, produciendo así corrientes eléctricas.
Características del electrón
- La masa del electrón es de 0,51 MeV/c2 o 9,1 × 10−31 kg. En comparación, la masa de un protón es unas 1836 veces más grande. De hecho, el electrón es una de las partículas más livianas que existen.
- Aunque tengan masa, los electrones no tienen un volumen asociado a ellos, y por ello, se representan como puntos.
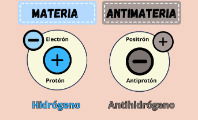
- La carga eléctrica de un electrón es negativa, con un valor de −1,602176 x 10-19 culombios. Esta carga contrarresta a la positiva del protón, de la misma magnitud pero de signo contrario.
- Los electrones orbitan dentro de una nube electrónica gracias a las fuerzas electromagnéticas, concretamente en orbitales. Los orbitales son espacios alrededor del núcleo atómico en el que hay una probabilidad alta de encontrar un electrón de nivel energético concreto.
- Los electrones pueden variar de nivel energético según ganan o pierden energía. Si ganan energía, saltan a un nivel energético superior, absorbiendo un fotón. Si pierden el fotón, emiten luz y bajan al nivel de energía original.
- Tienen un comportamiento ondulatorio, por lo que su movimiento describe una función de onda.
- El electrón es un leptón que, junto con el muon y tau, forma parte de la familia de los fermiones.
- Son partículas elementales con espín semientero o momento angular intrínseco de 1/2.
- Obedecen al principio de exclusión de Pauli, que establece que no puede haber dos fermiones en un mismo estado cuántico.
- Un átomo puede perder o ganar electrones, convirtiéndose así en un ion positivo o negativo.
- La tendencia de un átomo en ceder o absorber electrones se define como electronegatividad.
- Cuando hay flujo de electrones entre dos o más puntos, se genera corriente eléctrica y un campo eléctrico.
Vea también Configuración electrónica.
Descubrimiento del electrón
En 1891, el científico irlandés George Johnstone Stoney presentó la hipótesis de la existencia de estas partículas. En ella especulaba que tendrían carga eléctrica, y les asignó el nombre de electrón.
Sin embargo, fue Joseph John Thomson quien logró demostrar la existencia de los electrones en 1897. Mientras trabajaba en un estudio sobre los rayos catódicos, descubrió la existencia de unas partículas cargadas negativamente. Tras este hallazgo, Thomson elaboró su propio modelo atómico, denominado Modelo de Pudín de Pasas.
Entre 1907 y 1910, Robert Andrews Millikan, junto con Harvey Fletcher, realizó unos experimentos para determinar la carga del electrón. Se sirvió de gotas de agua y de aceite, y logró aproximar el valor de la carga, aunque con margen de error. Varios años después se logró establecer la carga con un valor más exacto, hasta llegar a 1,602176 x 10-19 culombios con seis decimales de exactitud.
Ver también:
Cómo citar: Significados, Equipo (17/11/2023). "Electrón". En: Significados.com. Disponible en: https://www.significados.com/electron/ Consultado: