Concentración química
La concentración química determina la cantidad de soluto y solvente en una solución química.
La concentración química es la proporción de las sustancias que se disuelven (solutos) en relación con la cantidad total de la solución. En este sentido, la cantidad de soluto siempre será menor al solvente para que se considere una solución.
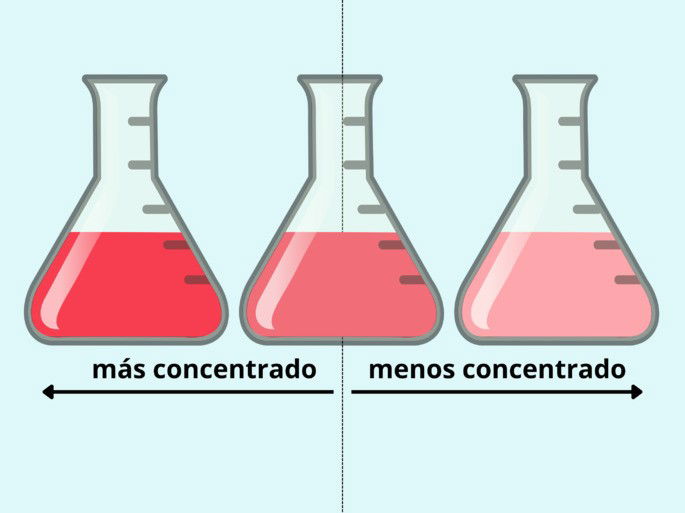
La preparación de una solución química requiere de calcular las medidas de soluto y solvente. Esto determinará la concentración de la solución y el tipo de solución. Las concentraciones de las soluciones se expresan por molaridad, molalidad o fracción molar, entre otros.
Medidas y fórmulas de concentración química
Las medidas de concentración de soluciones químicas son determinadas por unidades físicas y unidades químicas de concentración.
Por un lado, las unidades físicas son aquellas que definen la proporción entre el soluto y el solvente en masa, volumen o sus partes.
Las unidades químicas, por otro lado, definen la concentración de la solución por moles o equivalentes químicos que presenta el solvente.
Unidades físicas de concentración de soluciones
Las unidades físicas de concentración de soluciones expresan la proporción de soluto en peso, volumen o partes. Esta proporción se calcula siempre con respecto a la cantidad total de la solución.
Las fórmulas para calcular el porcentaje en masa o peso, o sea, su concentración, divide la cantidad de soluto por la de la solución. Finalmente, el resultado se suele multiplicar por 100.
Las medidas físicas de las concentraciones químicas y sus fórmulas son las siguientes:
Masa sobre masa
Masa sobre masa (%m/m), o también peso sobre peso (%p/p) expresa el porcentaje de masa o peso de soluto en relación con a la masa o peso de solución.
Volumen sobre volumen
Volumen por volumen (%v/v) indica la proporción del volumen del soluto en el volumen total de la solución.
Masa sobre volumen
Masa sobre volumen (%m/v), o peso sobre volumen (%p/v), representa la masa o peso del soluto respecto al volumen de la solución.
Partes por millón
Partes por millón (ppm) calcula los miligramos de soluto por kilogramos de solución. En este caso, el resultado se multiplica por un millón.
Unidades químicas de concentración de soluciones
Las unidades químicas de concentración de soluciones calculan la cantidad de moles o de equivalentes químicos de un soluto en una solución.
Las medidas químicas de concentración y sus respectivas fórmulas son:
Molaridad
La molaridad es el número de moles de soluto en litros de solución. Un mol es una cantidad de átomos de carbono expresado en la constante de Avogadro.
Para determinar el número de moles del soluto, es necesario conocer la masa molar de los elementos. Para ello, basta consultar una tabla periódica. La masa molar que se encuentra debajo del símbolo químico del elemento y también es conocida como masa atómica.
Puedes calcular la molaridad de una solución con la fórmula siguiente:
Para determinar el número de moles de un soluto, puedes emplear la siguiente fórmula:
En este caso, el número de moles se calcula dividiendo la masa de soluto por la masa molar de soluto. Para la masa molar, tendrás que sumar el total de todos los elementos que componen el soluto.
Por ejemplo, si el soluto es NaCl, deberás sumar las masas molares o atómicas de los elementos. El sodio, Na, tiene una masa molar de 22,99 g/mol, mientras que el cloro, Cl, tiene 35,45 g/mol. En conjunto, el soluto tiene una masa molar de 58,44 g/mol.
Vea también Masa molar.
Molalidad
Para calcular la molalidad, se utiliza la siguiente fórmula:
Para el cálculo de moles de un soluto se busca la masa atómica o masa molar que se encuentra debajo de cada elemento químico de la tabla periódica.
Normalidad
La normalidad es el número de equivalentes químicos (EQ) en un gramo de soluto contenido en un litro de solución. Los equivalentes químicos son la cantidad de sustancia que reacciona para producir un mol de producto.
La normalidad también es conocida como concentración normal y se calcula usando la siguiente fórmula:
Para calcular el equivalente químico (EQ) de un soluto se debe tener en cuenta si el soluto es un ácido o un hidróxido (OH) y el uso de las siguientes fórmulas según el soluto que corresponda:
Vea también:
Cómo citar: Significados, Equipo (20/03/2025). "Concentración química". En: Significados.com. Disponible en: https://www.significados.com/concentracion-quimica/ Consultado: